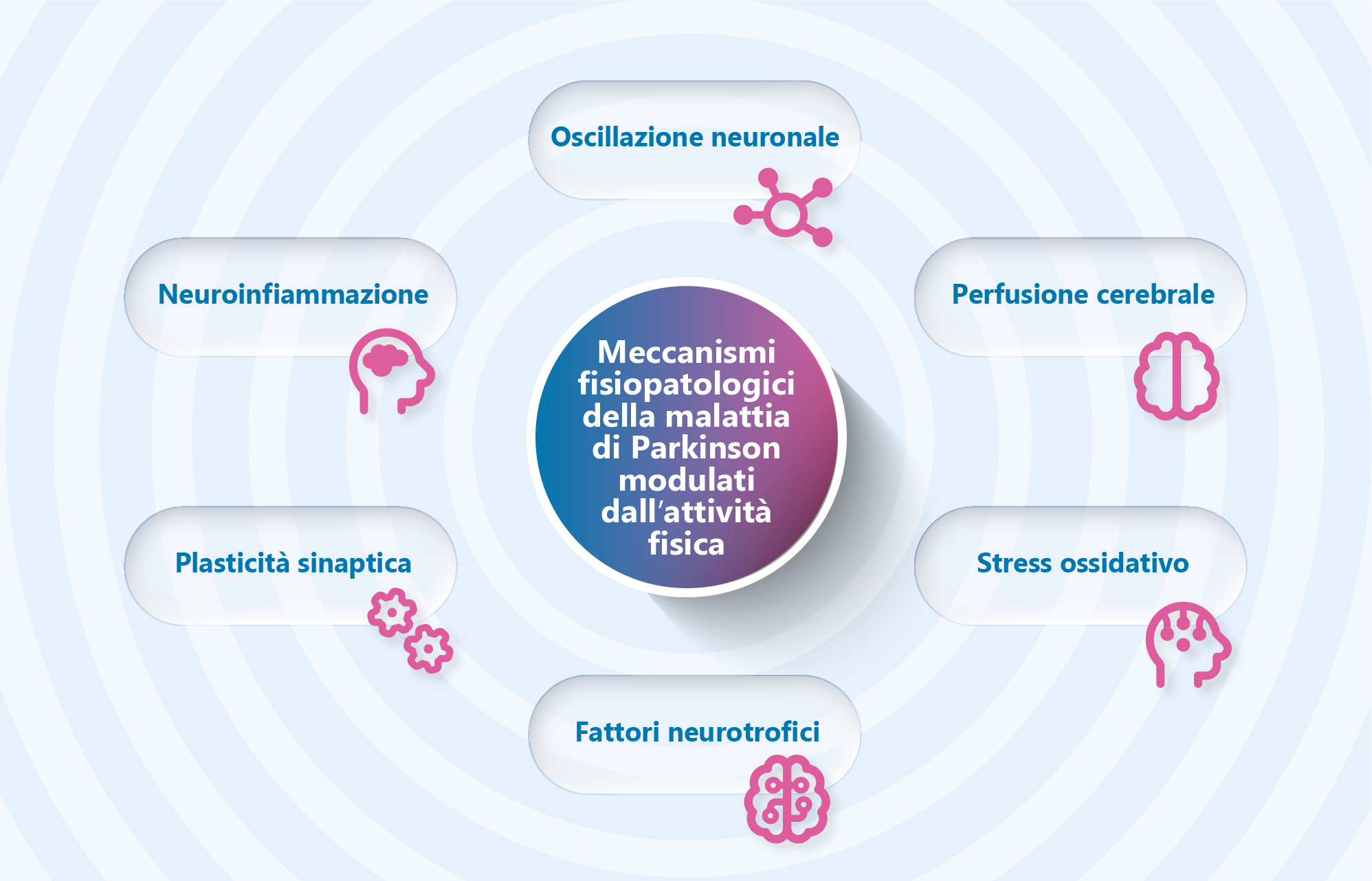
Modificato da Fig. 1, Wilson AC, Pountney DL, Khoo TK, Int J Mol Sci 2025;26(10):4860
Valutazioni su modelli animali hanno evidenziato un aumento dei livelli dei fattori neurotrofici endogeni dopo esercizio fisico indipendentemente dal grado di gravità di malattia.
I fattori neurotrofici mostrano un ampio ventaglio di attività neuroprotettive, dalla promozione della proliferazione e della sopravvivenza neuronale, alla formazione delle sinapsi, sino alla riduzione dell’aggregazione dell’α-sinucleina. Esistono tre grandi “famiglie” di fattori neurotrofici legati alla malattia di Parkinson: i brain-derived neurotrophic factor (BDNF), i glial cell line-derived neurotrophic factor (GDNF) e i cerebral dopamine neurotrophic factor/mesencephalic astrocyte-derived neurotrophic factor (CDNF/MANF).
Altri studi hanno dimostrato che l’attività fisica può modulare la plasticità sinaptica nelle regioni cerebrali colpite dalla malattia di Parkinson, agendo in particolare sull’input glutammatergico nei gangli della base e sulla neurotrasmissione dopaminergica all’interno di tali strutture.
La perdita dell’input dopaminergico della substantia nigra pars compacta verso lo striato, infatti, distrugge l’omeostasi della neurotrasmissione di dopamina e glutammato.
L’esercizio fisico sembra intervenire a questo livello riducendo la quantità di glutammato nella fessura sinaptica e ristabilendo la corretta densità delle spine dendritiche.
Benché non sia ancora stato chiarito quali siano le migliori tipologie e intensità di esercizio fisico per favorire la plasticità sinaptica, diversi studi hanno riscontrato una correlazione positiva con l’esercizio aerobico di intensità alta o moderata.
I deficit funzionali nella malattia di Parkinson si associano ad anomalie nell’attività oscillatoria dei neuroni nei gangli della base. È stato osservato che l’esercizio fisico esercita un impatto positivo su tale attività non solo in soggetti con malattia di Parkinson e modelli animali, ma anche in soggetti sani. In particolare è stato rilevato un miglioramento dell’attenzione, che potrebbe contribuire ad alleviare i sintomi non motori come deterioramento cognitivo ed eccessiva sonnolenza diurna.
La perdita dei neuroni dopaminergici che si riscontra in corso di malattia di Parkinson determina una riduzione della circolazione sanguigna nelle aree circostanti, che può aggravare ulteriormente la condizione portando allo sviluppo di infiammazione e di disfunzioni metaboliche oltre che a un aumentato accumulo di ferro, con conseguenti sintomi motori e non motori.
Benché siano pochi gli studi che hanno valutato in modo specifico il legame fra esercizio fisico e perfusione cerebrale nella malattia di Parkinson, è noto che l’esercizio fisico può modulare il flusso sanguigno cerebrale, giustificando così l’impatto positivo dell’esercizio sui sintomi della malattia.
Anomalie nella perfusione cerebrale si presentano precocemente nella malattia di Parkinson e correlano con una disfunzione esecutiva.
La neuroinfiammazione è saldamente legata allo sviluppo della malattia di Parkinson. Soprattutto in modelli animali è stato osservato che l’attività fisica, anche di intensità bassa o moderata, è in grado di up-regolare citochine antinfiammatorie come IL-10 e TGF-β. Quest’ultimo è un importante regolatore dell’attività della microglia in grado di favorire il passaggio dallo stato di attivazione pro-infiammatoria a quello di stato anti-infiammatorio e neuroprotettivo, riducendo quindi la risposta infiammatoria.
Infine sta diventando sempre più evidente l’importante ruolo della disfunzione dei mitocondri e del conseguente aumento delle specie reattive dell’ossigeno (ROS) nella degenerazione dopaminergica nella malattia di Parkinson. È ampiamente noto che la contrazione muscolare genera ROS – quindi si potrebbe ipotizzare un effetto deleterio dell’esercizio fisico – ma in realtà questo avviene unicamente fino a un livello soglia che attiva un effetto adattativo: la fatica muscolare e lo sforzo cardiovascolare proteggono quindi i tessuti dai danni associati a livelli eccessivi di ROS. Questo effetto adattativo potrebbe giustificare il diminuito stress ossidativo e l’aumentato livello ematico di antiossidanti registrati dopo l’esercizio fisico in diversi studi su soggetti con malattia di Parkinson.
In conclusione sembra di poter affermare che l’esercizio fisico abbia vari effetti positivi sui sintomi motori e non motori della malattia di Parkinson: servono tuttavia maggiori studi condotti sull’uomo per stabilire la tipologia e l’intensità di esercizio più adatte ai singoli stadi di malattia.